- Загадки биологии - часть: 1 2 3 4
Как самоупаковывается белок?
Белки — основной материал, из которого состоят живые клетки. Они представляют собой различные комбинаций веществ, называемых аминокислотами. Все эти аминокислоты присутствуют в каждой клетке.
Как молекуле белка удается быстро сворачиваться единственно верным способом?
Белки являются очень сложными молекулами с многоуровневой структурой и сложнейшими функциями. Например, гемоглобин переносит кислород в крови, а инсулин помогает перерабатывать сахар.
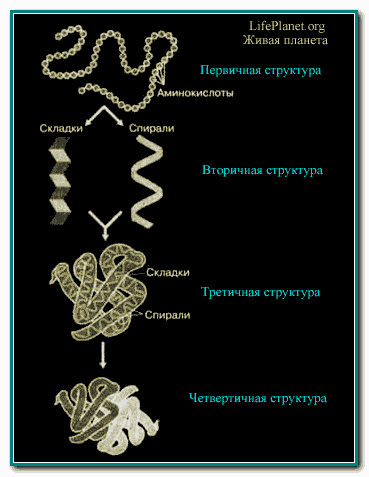
Рис. 1. Уровни внутренней структуры белка.
Если развернуть структуру белка, как клубок с нитками, то можно заметить, что он свернут не хаотически, а в строго упорядоченной последовательности. Во внутренней структуре свертки белка в плотно упакованный клубок учёные научились выделять следующие уровни (см. рис. 1):
- первичная структура— цепочка аминокислот, связанная пептидными связями;
- вторичная структура — спираль, связанная водородными связями;
- третичная структура — отдельные фрагменты складок или спирали связаны дополнительными связями;
- четвертичная структура — несколько цепочек аминокислот связаны друг с другом.
На самом глубинном уровне все белки состоят из цепочек 20 разных аминокислот, причём именно порядок аминокислот, заданный ДНК, определяет предназначение того или иного белка (см. рис. 2).

Рис. 2. Схема строения первичной структуры белка:
цепочка из 20 разных аминокислот, которые связаны друг с другом пептидными связями.
Вот как выглядит процесс генерации белка в общем.
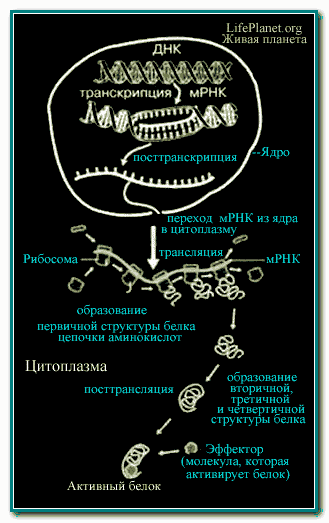
Рис. 3. Схема синтеза и самосборки белка.
Как уже упоминалось выше, на этапе транскрипции внутри ядра клетки (рис. 3) гены (ДНК) транскрибируются (переписываются) в РНК. Затем на этапе посттранскрипции РНК преобразуется в информационную (или матричную) мРНК; далее мРНК попадает в цитоплазму, где рибосомами транслируется в белок. Наконец, на этапах трансляции и посттрансляции формируется сложная структура белка.
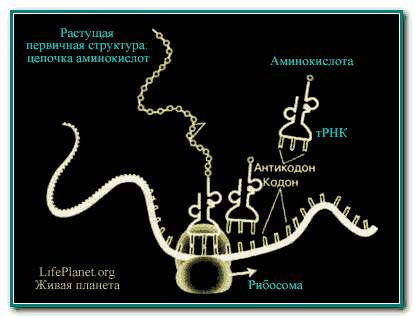
Рис. 4. Процесс образования первичной структуры белка,
когда две или более аминокислоты связываются пептидными связями в цепочку аминокислот.
В процессе трансляции образуется самый первый уровень структуры белка, а именно первичная структура, т.е. цепочка амино-кислот, связанная пептидными связями (рис. 4). Далее на этапе посттрансляции происходит самый загадочный и интересный процесс, а именно фолдинг (сворачивание или самосборка) белка с образованием следующих уровней: вторичного, третичного и четвертичного.
Из бесконечного количества возможных вариантов фолдинга (свертки) молекула белка выбирает единственно правильный всего за несколько долей секунды. Если поставить компьютеру такую задачу перебора всех возможных вариантов, то для её решения потребуется невероятно много времени!
Задача определения свертки белка — одна из самых сложных задач в современной биологии. Как природе практически мгновенно удается решать аналогичную задачу для множества разных молекул белка, а именно свертывать их единственно верным способом? Учёным ещё только предстоит найти ответ на этот вопрос.
Исторически важные этапы изучения свойств белка.
1838 г. — шведский химик Йене Якоб Берцелиус (Jons Jakob Berzelius) предложил термин протеин (используется как синоним термина «белок») от греческого слова (прота), означающего «первостепенной важности».
1902 г.— Франц Хофмайстер (Franz Hofmeister) и Эмиль Фишер (Emil Fischer) впервые предложили правильную теорию строения белка как линейной полимерной цепочки из аминокислот, связанных пептидными связями.
1926 г. — Джеймс Самнер (James Sumner) доказал, что энзим уреаза (urease) является белком, и кристаллизовал его.
1929 г. — Джон Говард Нортроп (John Howard Northrop) изолировал и кристаллизовал энзим пепсин (pepsin) и доказал, что он является белком.
1946 г. — Джон Говард Нортроп и Уэнделл Мередит Стэнли (Wendell Meredith Stanley) удостоены Нобелевской премии по химии «За получение в чистом виде энзимов и вирусных белков», а Джеймс Самнер — «За открытие явления кристаллизации энзимов».
1958 г. — Макс Перуц (Max Perutz) и Джон Кодри Кендрю (John Cowdery Kendrew) впервые определили структуру белка (миоглобина).
1944-1955 гг. — Фредерик Сенгер (Frederick Sanger), изучая структуру инсулина, разработал метод идентификации, с помощью которого ему удалось установить природу и последовательность чередования аминокислот в белке инсулине и расшифровать его строение. Эти работы послужили основой для синтетического получения инсулина и других гормонов.
1958 г. — Фредерик Сенгер получил Нобелевскую премию по химии «За установление структур белков, особенно инсулина».
1962 г.— Макс Перуц и Джон Кодри Кендрю получили Нобелевскую премию по химии «За исследования структуры глобулярных белков».
1971 г. — основан международный банк данных белков Protein Data Bank.
2004г.— Аарон Цехановер (Aaron Ciechanover), Авраам Гершко (Avram Hershko) и Ирвин Роуз (Irwin Rose) получили Нобелевскую премию по химии «За открытие убиквитин-опосредованного (ubiquitin-mediated) разложения белка».
LifePlanet.org
- Загадки биологии - часть: 1 2 3 4



